摘要:可再生能源在利用过程中存在瞬时性、不稳定性以及供应与需求不匹配等问题。热化学储热技术具有储能密度大、储热温度高等特点,能够实现高效长时储热,可以将不稳定的可再生能源转化为稳定的中高温热能,并满足用户侧的波动需求。针对工作温度范围为400~1 100℃的中高温热化学储热材料,阐述了其分类、基本原理和特点,系统总结了碳酸盐、氢氧化物、氧化物、金属氢化物、氨和甲烷等典型热化学储热材料及其储热性能,分析了其结构定向调控及改性方法,并对典型的工程应用进行了介绍;分析了固-气和气-气反应体系的反应器设计及系统集成的研究进展,并针对优质热化学储能材料在开发及工业应用方面存在的问题,指出了未来的发展方向。
目前,常规热能主要来源于煤、石油、天然气等传统化石燃料燃烧。随着化石燃料消耗加剧以及环境污染日益严重,发展可再生能源,促进碳减排,实现碳中和,已经成为世界各国达成的共识。然而,在太阳能等可再生能源利用过程中仍面临瞬时性及不稳定性、供应与需求不匹配等问题。例如,太阳能发电受天气、季节、光强等影响极大;生物质热转化可以持续稳定产生大量中高温热量,但用户需求随时空变化较大、波动性强。如何将间歇性能源转化为可以持续稳定输出的热能,并满足用户侧波动需求,是可再生能源推广应用亟待解决的关键问题。
热能储存技术能将不稳定的太阳能或高温余热等能量转化为储热介质中的热能和化学能,然后根据需要释放热能,保证用户侧能源需求。储热系统与能源系统的耦合是克服每日、每周甚至季节性能源需求和供应不平衡的一种行之有效的方法,因此,高效且具有成本效益的热能储存技术对于推动能源革命和引领能源业态发展新方向发挥着重要作用。
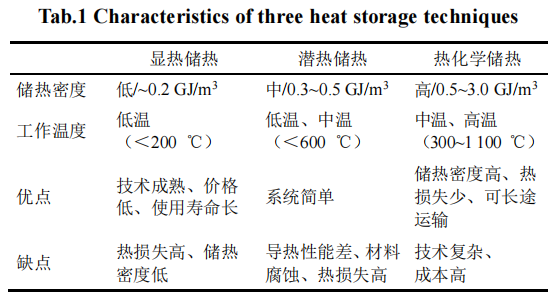
储热技术包括显热储热、潜热储热和热化学储热。表1对比了3种储热方式的特点。与显热和潜热储热相比,热化学储热具有以下优势:1)储热密度高达0.5~3.0 GJ/m3,是显热或相变储热的5~10倍;2)工作温度范围一般在400~1 100℃,能够有效存储中高温热能;3)反应物和产物可以在环境温度或工作温度下保存,能够实现热能的长期高效储存;4)反应温度窗口较宽,如NH3/N2+H2或Ca(OH)2/CaO+H2O,正-逆反应可在350~600℃下进行,能够有效提升热能品质。
表1 3种储热技术的特点
储热材料是影响热化学储热性能的关键。一般而言,在经历多个储/放热循环后,储热材料的性能会发生一定的衰减。因此,寻找和优化具有转化率高、可逆性好、反应速率快、储热密度大和循环稳定性强的储热材料对热化学储热技术的发展至关重要。基于此,本文将分析热化学储热机理,重点对储热材料类型及性能进行分析,介绍典型示范工程、反应器和系统设计,并对未来发展趋势进行展望。
1热化学储热基本原理
热化学储热技术是一种基于可逆化学反应的储热方式,通过化学物质的合成与分解来储存和释放热量,其反应通式为:
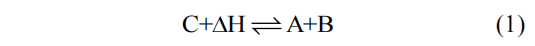
在该反应中,储热材料C通过吸收太阳能、高温余热等能量转化为A和B,经过换热器回收显热后分别独立储存。当需要释放能量时,A和B经过预热后直接接触,发生逆向反应合成C,并将储存的化学能转换为热能释放出来。通过构建闭环系统并妥善保存储热介质,可以实现长时间无损储热。
基于上述原理,高性能热化学储热系统一般具备以下条件。首先,反应过程需要具有较好的可逆性,没有明显副反应的发生,以保证储/放热前后反应物的一致性,从而有效降低储热性能衰减;其次,正逆反应速率均较快,能够实现热量的快速存储和释放;最后,反应物具有易分离的特点,且能够稳定存储。此外,反应物应为无毒无害、无腐蚀性物质,这对于技术的规模化工业应用也极为重要。
目前,热化学储热材料种类较多,主要可归纳为碳酸盐、氢氧化物、氧化物、金属氢化物、氨和甲烷等6类[8](图1)。一些常见储热材料的反应温度和储热密度列于图2。由图2可见,氨的体积储热密度为745 kW·h/m3,而甲烷则具有较高的质量储热密度,达4.34 kW·h/kg。
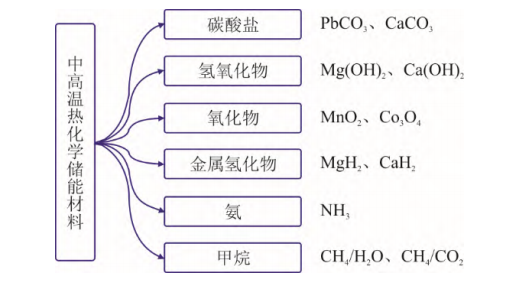
图1热化学储热候选材料
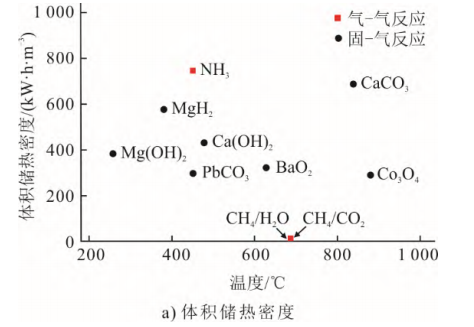
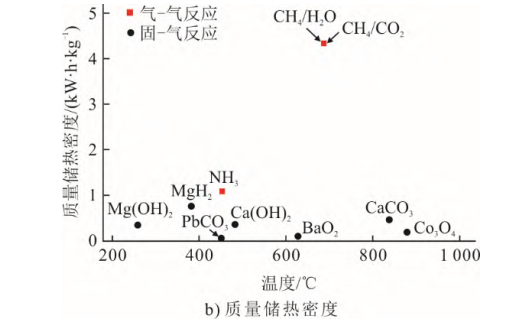
图2不同材料的反应温度与储热密度
2热化学储热材料
2.1碳酸盐
碳酸盐储热材料通过煅烧/碳酸化反应实现热量的储存/释放(式(2))。碳酸盐通过煅烧形成相应的氧化物和CO2,实现能量存储。在碳酸化过程中,碳酸化反应器能够直接集成在动力循环中,成为一个封闭系统,通入碳酸化反应器的高压低温CO2流量远超化学反应所需的量,在化学反应放热作用下,未反应的过量CO2直接作为工质实现热量传递。
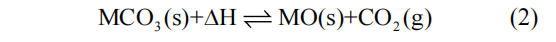
目前,主要的碳酸盐储热材料包括CaCO3/CaO、SrCO3/SrO、PbCO3/PbO、BaCO3/BaO等。然而,BaO在碳酸化反应过程中可能发生其他副反应,形成共晶混合物,导致反应无法完全可逆。PbCO3/PbO储热密度可达1.6 GJ/m3,但Pb是一种毒性较高的重金属元素,因此,PbCO3/PbO储热材料的应用对人体健康和环境具有潜在的毒害风险。相比较而言,CaCO3/CaO和SrCO3/SrO不仅具有较高的储热密度,分别可达3.26、4.00 GJ/m3,而且在反应过程中没有其他副反应,材料无毒无害,应用前景十分广阔。
CaCO3/CaO主要来自于石灰石等天然矿石,自然界储量十分丰富,成本也较低,是当前研究最多的碳酸盐储热材料。然而,CaCO3/CaO直接作为储热材料时,在高温下CaO由于晶粒增长和孔隙减少会发生烧结,导致CO2扩散受限,其储热密度也随着循环次数的增加迅速下降。目前,相关研究主要集中于对CaCO3/CaO改性以提高其循环稳定性。惰性载体(如SiO2、Al2O3、MgO、TiO2等)负载是一种常用的抑制CaCO3/CaO材料烧结的有效手段。如CaO可以和Al2O3通过固-固反应生成Ca3Al2O6、Ca3Al10O18、Ca9Al6O18和Ca12Al14O33等铝酸钙,它们都是有效的惰性支撑材料,在储/放热过程中不参与可逆反应,但可以作为间隔物有效防止钙基材料晶体的增长和颗粒之间的接触,从而抵抗烧结。Sun等人[15]采用湿式混合法制备了CaO/质量分数5%Al2O3复合材料。结果表明,该复合材料的初始储热密度为2 288 kJ/kg,是CaO的1.24倍。同时,得益于Ca12Al14O33对CaO结构的支撑作用,在循环30次后,复合材料的储热密度仅下降至初始值的68%,而相同情况下纯CaO则下降了80%。
此外,在碳酸化反应过程中,由于CaCO3的摩尔体积(34.1 cm3/mol)高于CaO(16.9 cm3/mol),CaCO3产物层将首先覆盖CaO固体表面,并逐渐阻碍CaO和CO2的直接接触。丰富的介孔/大孔结构能够承受储/放热循环过程中发生的剧烈体积变化,从而促进CO2在CaO内的扩散,提高反应物活性,有效提升抗烧结性能。为制备多孔CaO,一般可以选用有机钙前驱体(甘氨酸钙、甲酸钙、乙酸钙、柠檬酸钙等)为原料,在煅烧过程中,有机组分的分解挥发会形成大量的孔隙。Xu等人以甘氨酸钙制备的CaO比表面积和孔容可达10.66 m2/g和0.055 cm3/g,远高于CaO的0.78 m2/g和0.004 cm3/g。在60次650℃煅烧/900℃碳酸化循环中,甘氨酸钙煅烧产生的CaO累计储热密度为110.124 kJ/g,约为未改性CaO的6倍,储热性能显著提升。
通过负载惰性载体以抵抗钙基材料烧结和团聚的方式已经被研究了很多年,但仍然没有复合材料投入商业使用。这是因为相关研究主要集中在基于热重实验的基础理论研究,尚未开展超过1 000次循环的实验测试。因此,亟需进一步对储热材料改性方式及制备工艺进行优化,开发性能优异、成本低廉、工艺简单、可大规模生产的储热材料,并在实际应用条件下开展长周期循环测试。
2.2氢氧化物
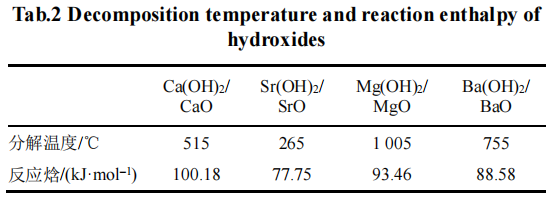
氢氧化物储热材料的储热原理与碳酸盐相似,主要利用水(蒸汽)和金属氧化物(碱金属和碱土金属)之间的反应实现热量的储存及释放(式(3))。
常见的氢氧化物储热材料主要包括Ca(OH)2/CaO、Sr(OH)2/SrO、Mg(OH)2/MgO和Ba(OH)2/BaO等,它们的分解温度和反应焓见表2。Ca(OH)2/CaO是一种中温储热材料,其分解温度为515℃。与其他几种氢氧化物相比,Ca(OH)2/CaO反应焓值最高,储热密度大,且具有安全无毒且成本低廉等特点,是当前最重要的氢氧化物储热材料。
表2氢氧化物的分解温度和反应焓
然而,在热量储/放循环过程中,Ca(OH)2颗粒会逐渐吸附周围颗粒,形成块状团聚体,引起材料床层特性发生变化,严重影响传质与传热,从而降低反应物活性和循环稳定性。Dai等人探究了粉末状Ca(OH)2/CaO在填充床反应器中的水合/脱水特性。在脱水过程中,最初70 min内,反应器外部温度始终高于内部温度,在70~180 min内反应器内部温度反而更高;在水合过程中,反应器中心最高温度可达475℃,下降速度较慢,且内部温度始终高于外部,表明加热和放热过程中存在严重的热滞后现象。这主要是因为反应物的团聚导致反应床渗透性变差,不仅使反应器内压降过于迅速,还在放热反应过程中阻碍水蒸气与反应物的有效接触。
为此,学者们通过在Ca(OH)2/CaO中掺入SiO2、膨胀石墨、六方氮化硼等高导热材料,增强其传质传热性能,降低团聚效应。Huang等人制备了含有质量分数15%六方氮化硼的Ca(OH)2,在300℃时其热导率提升了22.9%,脱水焓也由109.3 kJ/mol上升至115.9 kJ/mol。经过10次脱水/再水化循环后,该材料仍能保持67%转化率和大于1 000 kJ/kg的能量密度,比纯Ca(OH)2高出9.8%。此外,将Ca(OH)2/CaO粉末制备成颗粒材料,以减少Ca(OH)2粉末间的吸引力,同样也能增强其循环稳定性。Afflerbach等人采用氧化物陶瓷外壳包覆Ca(OH)2/CaO,其压碎强度增加了17.8%,达到105.3 N,同时其热导率也提高了60%。改性材料的转化率在第4个循环后逐渐稳定,且稳定性十分良好。
机械性能差被认为是氢氧化物循环寿命衰减的主要原因。添加惰性材料是缓解团聚的方法之一,但性能衰减仍难以满足实际应用需求。因此,需要进一步从微观角度探索改性氢氧化物自身性能与循环寿命之间的关系,揭示惰性材料在储/放热过程中的作用。此外,氢氧化物储热系统是一种化学反应与传热的动态耦合技术,为满足工业化储热需求,还应加强系统集成层面的研究,重视经济性分析。
2.3氧化物
氧化物储热材料主要为Co3O4/CoO、Mn2O3/Mn3O4、Pb3O4/PbO和CuO/Cu2O等多价态过渡金属氧化物。在储热过程中,高价金属氧化物在高温下吸热分解,生成低价金属氧化物;而热量的释放则通过低价金属氧化物与氧气发生氧化反应实现(式(4))。金属氧化物的氧化还原反应焓普遍较高,反应温度通常在600~1 000℃,特别适用于高温热能存储。
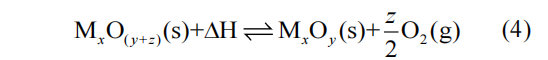
一般而言,Co3O4/CoO在等温变压循环下可逆性较高,不易出现性能衰减或损失;而Pb3O4因在温度低于550℃时难以发生分解反应,无法实现能量存储,仅适用于650℃以上的储热场景,而且存在较多副反应。此外,Co3O4/CoO和Pb3O4/PbO均为具有较高生物毒性材料,这也极大地限制了其实际应用。对于CuO/Cu2O,其反应焓可达404.67 kJ/mol,但当温度接近1 200℃时CuO/Cu2O会出现相变,其熔融状态具有腐蚀性。相比较而言,Mn2O3/Mn3O4是目前最理想的氧化物储热材料。Mn2O3/Mn3O4具有理论反应焓高(为202 kJ/kg),原料易得、毒性低和成本低廉等优势。
在储/放热循环过程中,Mn2O3/Mn3O4也会由于晶体结构逐渐致密化而发生烧结,并伴随着黑锰矿相(MnMn2O4)的形成,降低能够有效参与氧化反应Mn2O3/Mn3O4的含量,从而致使其储热性能逐渐降低。为提升反应可逆性,可以在Mn2O3中掺杂硅氧化物。Si4+会导致晶格畸变,从而引发缺陷,提高晶格氧和缺陷氧的比例,降低表面氧吸附和氧解离的反应能垒,而且晶体内部的氧迁移能垒也会明显降低,这都有利于提高储热稳定性[27]。Bielsa等人通过溶胶-凝胶法合成了1 mol%和5 mol%Si掺杂的Mn2O3,经历40个循环后,其再氧化率仍分别高达99.93%和99.74%,烧结得到显著抑制。
金属氧化物储热体系的储能密度可高达1 000 kJ/kg以上,理论上具有良好的可行性和应用前景,但相关研究仍处于早期阶段。为了扩宽整个储热系统的温度操作窗口,未来研究将着重聚焦于制备混合氧化物(Co-Mn、Mn-Fe等),并改善材料的循环稳定性和反应动力学,降低合成成本。此外,还应通过理论计算等手段阐述混合氧化物反应之间的复杂关系。
2.4金属氢化物
金属氢化物是指Li、Na、Mg、Ti等金属元素与氢元素组成的化合物,在过去几十年中通常被用作储氢材料。金属氢化物在吸/脱氢过程中会伴随着大量热能的释放与吸收,反应温度为200~700℃(式(5))。
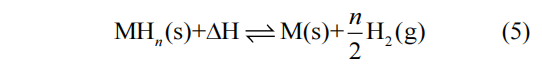
目前,金属氢化物热化学储热材料包括LiH/Li、MgH2/Mg、TiH2/Ti、CaH2/Ca。其中,Mg基储热材料价格低廉,原料来源丰富,储氢能力强,是最有发展前景的储氢介质。
一般而言,金属氢化物的反应速率较慢,这是限制其大规模应用的关键因素。高能球磨、化学沉积或等离子球磨等方法能够将金属氢化物制备成粒径在3~50 nm的纳米颗粒,通过增加其比表面积加速H2吸/脱附过程。在吸氢反应过程中,纳米颗粒晶界上氢原子的比例也会增加,从而加快H2扩散速率。然而,在反复的吸氢/脱氢循环过程中,由于温度和压力的变化,纳米颗粒仍会发生团聚,其储热性能随之下降。碳气凝胶、介孔碳(CMK3)和分子筛(SBA-15)等基材可以约束纳米颗粒,有利于阻止晶粒生长并保持纳米结构的稳定性。Soni等人将Ti、Ni、Fe共负载在石墨烯上(Ti-Ni-Fe Gr),并通过球磨法将其引入MgH2中以改善其储氢性能。实验结果表明,MgH2-Ti-Ni-Fe Gr初始分解温度降低到252℃,在50 s内吸收质量分数5.60%H2,在8 min内析氢能力为5.70%(质量分数)。同时,MgH2-Ti-Ni-Fe Gr具有极佳的循环稳定性,在循环24次后仅衰减了不足0.25%(质量分数)。这种方法虽然能够提高金属氢化物的循环次数,但由于负载能力有限,纳米固化MgH2的储氢能力仍会逐渐下降。
在金属氢化物中添加单一或复合金属(Al、Na、La、Ag等)可以降低反应能垒,也是提高其吸/脱氢速率的有效途径。Kumar等人基于第一性原理计算发现,在MgH2掺入Al和Sc不仅可以使其分解温度由140℃分别下降至52℃和132℃,而且还能保持与MgH2相似的体积模量和质量密度(7.61%和7.3%)。Lu等人合成的三元复合材料MB-5(质量分数90%MgH2+质量分数5%AlH3+质量分数5%NaBH4)具有更好的脱氢动力学和循环性能。实验结果表明,MB-5在9 min内能释放质量分数6.8%的H2,而MgH2则需要30 min以上才能释放出相同数量H2。此外,MB-5具有良好的循环特性,在第10次循环仍可保持6.35%(质量分数)的可逆储氢容量。
目前,金属氢化物主要应用于聚光太阳能储热,并开展了示范应用。澳大利亚EMC solar公司于2010年设计了一套采用CaH2作为储热材料的可调度聚光集热发电站,可持续输出100 kW的电力,并制造了一个容量为50 kg CaH2的反应器,测试结果证实CaH2具有良好储能密度和反应动力学性能。总体而言,从目前的研究进展来看,由于金属氢化物材料自身性质限制,这些材料还不能完全满足商业应用需求。因此,未来的研究工作仍需聚焦金属氢化物材料的开发及改性优化,特别是从微观角度解释复合金属氢化物的改性方法,基于分子动力学或DFT的理论计算深入了解微观尺度储/放热特性和循环行为,指导设计具有稳定循环寿命的金属氢化物材料。
2.5氨
20世纪70年代,澳大利亚国立大学基于氨的可逆解离提出用于聚光集热发电的氨基热化学储热概念,距今已发展50余年(式(6))。
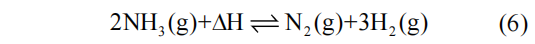
氨基热化学储热系统的组成如图3所示。反应器中的NH3在600~800℃下分解成H2和N2,并直接保存在储罐内。2种气体可以随时通过氨合成反应器,释放热量用于供热并补充氨的存量,放热步骤通常在350~550℃进行。氨具有较高的储热能力,在20 MPa和25℃时,其反应焓为66.8 kJ/mol,相当于每1 kg NH3可储热1.09 kW·h。同时,该系统不仅易于控制,没有其他副反应,而且NH3、H2和N2可自动发生相分离并储存于同一个储罐中,减少设备建设和维护成本。
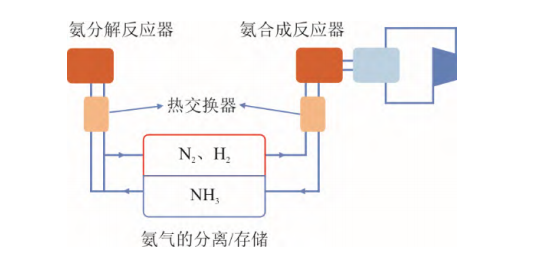
图3氨热化学储热系统
然而,氨分解反应能垒较高,在常规条件下反应速率较慢。为了促进NH3裂解反应,通常需要提高温度并使用催化剂。常用的催化剂包括Ru基催化剂、过渡金属催化剂及双金属催化剂。Ru基催化剂与NH3具有最适当的Ru-N结合能,在氨分解反应中表现出优异的催化性能,能够有效地加速NH3分解。Zhang等人制备的Ru/Pr2O3催化剂在温度为450℃、空速为30 000 ml/(g·h)时,可使H2产率达到20.9 mmol/(g·min),并在100 h内保持高活性。
尽管如此,Ru由于价格高昂且稀缺,其应用受到了极大的限制。相比较而言,Co是一种相对丰富的资源,而且Co基催化剂与NH3的Co-N结合能与Ru-N结合能较为接近,其催化活性也较高,因此Co基催化剂在氨分解领域具有较高的研究价值。Li等人在600℃下直接热解ZIF-67前驱体制备了Co/NC-600催化剂。在反应温度为500℃、空速为30 000 ml/(g·h)时,Co/NC-600实现了80%的NH3转化率,并保持72 h不衰减。
氨合成是基于Haber-Bosch工艺的成熟技术,相关研究可为提高系统循环寿命提供充分参考。然而,现有的催化技术难以实现正向反应和逆向反应完全转化,这导致其在商业应用中吸收和释放的热能较理论计算有所减少。当前的研究主要通过分析热力学参数和催化类型对氨合成的影响来确定最佳反应条件,但相关微观反应机理仍不清楚。因此,需要进一步研究从微观角度提高正向和反向反应的转化率,指导新型催化剂的开发,形成有针对性的催化剂优化合成策略,改善储放热过程中反应的可逆性,从而提升储热性能。
2.6甲烷
甲烷重整反应主要用于合成气或氢气的生产,其反应焓值通常较高,所以能够借此实现热能的存储及释放。根据反应物的不同,甲烷重整反应可分为甲烷干重整(DRM)反应和甲烷水蒸气重整(SMR)反应。可逆化学反应及对应的副反应如式(7)—式(10)所示。
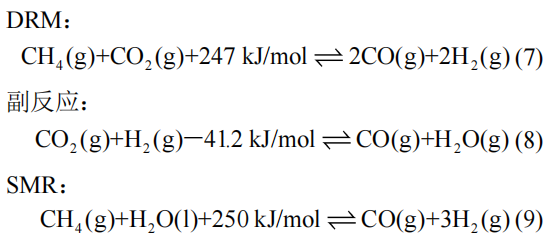
副反应:
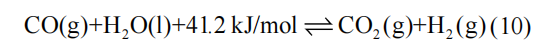
甲烷重整反应需要克服较高的反应能垒,通常在700℃以上的高温下才能进行,其反应效率很大程度上取决于催化剂性能。甲烷重整催化剂中使用的活性组分可分为Ni、Co等非贵金属以及Rh、Pt、Ru等贵金属。在重整反应过程中,Pt、Ru等贵金属催化剂具有优异的催化活性和抗结焦能力。Shen等人合成的Pt/CeO2催化剂在350℃下就能催化DRM反应,而且在10 h没有出现失活现象,具有较佳的抗结焦性能。然而,虽然贵金属具有良好的催化活性,但其存在原料来源少、价格昂贵、催化剂强度较低等不足,难以满足规模化应用需求。
Ni基催化剂是一种成本相对较低的非贵金属催化剂,对催化重整也具有良好的催化活性,已经广泛应用于天然气等有机物催化重整领域,但其在长周期高温运行条件下容易出现碳沉积和活性成分聚合的现象,致使催化效率显著降低。Co、Pb等表面活性组分可以对Ni基催化剂表面进行修饰,通过减少金属颗粒的相互作用避免催化剂失活。Wang等人通过模拟得出CH4和CO2在Ni-Co双金属DRM催化剂上具有较低的解离能垒,表明Ni-Co有助于提高催化剂的催化活性。DRM实验结果表明,Ni-Co催化剂经过100 h也未形成积碳。Batebi等人在Ni/Al2O3中添加Pd后,反应还原度从69.2%显著提高到83.1%,CH4转化率、H2和CO产率也有所增加,而且减少了催化剂焦炭沉积。
SMR反应体系首先于1975年被应用于核能的储存,反应流程如图4所示,其效率可达60%~73%。首座由太阳能驱动的SMR示范电站建立于澳大利亚的Tapio Station,其容量为50 MW。
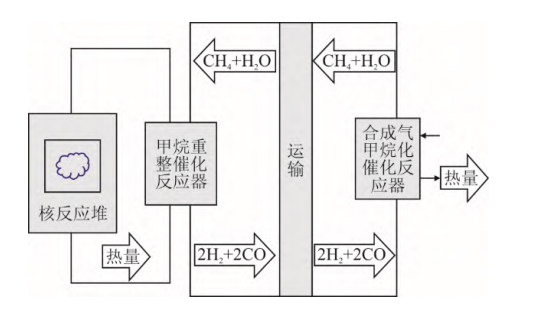
图4核能和SMR系统耦合的循环反应流程示意
该电站采用塔式聚光重整反应器制备合成气,通过燃气轮机推动透平发电。该系统已经在实际应用中验证了可行性。因此,该技术的研究重点是在工程应用的基础上研发抗积碳性能强、催化活性高的催化剂,进一步提升催化转化效率,降低生产成本。
3反应器设计及应用
3.1反应器设计
作为热化学储热系统的核心设备,热化学反应器直接影响实际储/放热效果。根据反应物的性质,反应器可分为固-气反应器和气-气反应器。
针对固-气反应,主要的反应器类型包括固定床、流化床和回转窑反应器等。其中,固定床是最常采用的反应器类型。在固定床反应器中,反应物装在反应器内,导热流体流经反应物进行换热。固定床具有易于设计、施工操作方便等特点,目前已被广泛应用于碳酸盐、氢氧化物、金属氢化物和氧化物等储能材料的实验研究和应用。与此同时,还开发了不同复杂程度的数值模型,用于系统诊断、结果评估和反应器设计改进。然而,固定床的导热性较低,导致传热缓慢,极大地限制了固定床反应器的应用。在热交换器壁上安装延伸至反应器内部的翅片,可显著增强床内的热传递。Ye等人提出了一种新型多孔树形翅片,有效提高Ca(OH)2/CaO反应器的传热和传质性能。在蓄热过程中,多孔树形翅片加速了水蒸气的排出,与径向翅片反应器相比,蓄热时间缩短了44.4%,放热时间缩短了48.4%。
气-气反应器主要分为直接加热式和间接加热式2种。在间接加热反应器中,热能通过不透明表面(即管或板)转移到反应物。间接加热气-气反应器主要是催化管式重整器,催化剂固定在管内,反应气体流过催化剂床层发生反应。然而,在反应过程中,由于反应器内部热分布不均匀,部分未反应的CH4会在系统中循环,会导致能源效率降低。因此,如何优化反应器结构,强化反应器内部热质传递,提高能源转化和利用效率,是本技术的研究重点。Yuan等人研究了操作条件和反应器结构对管式反应器中SMR储热性能的影响,当床层孔隙率为0.7~0.8、反应器直径为40 mm、出口温度为1 000℃时,热化学储热效率达到最大值35.6%,而显热储热效率和总能效将分别为38.3%和73.9%。
3.2应用
热化学储热技术在可再生能源利用、火电调峰和余热回收领域应用中具有广阔的前景。
在可再生能源利用领域,相较熔盐储热系统,热化学储热系统具有更高的储热密度和储热温度,可以进一步提高光热发电效率。以超临界CO2为传热介质的第三代聚光集热发电站工作温度可达700℃,通过耦合碳酸盐储热系统,可以将热-电效率提升至40%以上,工艺流程如图5所示。煅烧反应器在白天通过太阳能进行储热。碳酸化反应器直接集成在动力循环中,成为一个封闭的再生循环。流入碳酸化反应器的CO2流量大大超过了CaO碳酸化反应化学计量的需要,化学反应直接加热未反应的过量CO2,由其将碳酸化反应的热量传递至涡轮机做功发电。
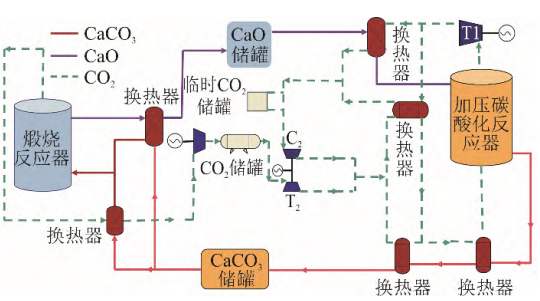
图5闭式CO2布雷顿循环CaO/CaCO3储热系统
在火电调峰领域,热化学储热系统可以提高火电机组深度调峰和提供高温蒸汽能力。在用电低谷时,抽取部分高温蒸汽或再热蒸汽通过热化学储热系统实现储热;或直接用电加热储热系统;也可以通过换热器将烟气中的高温余热回收及以上多种形式混合加热。待用电高峰时,直接生产高温蒸汽来推动透平发电。
在余热回收领域,热化学储热系统可以回收钢铁、水泥等工业生产过程中产生的间歇性废热。与区域供热系统合并后,能够生产稳定的高温蒸汽并向外供热。然而,上述系统集成均处于理论研究阶段,尚需进一步完善系统能量回收网络,推动多应用场景下能量储放工程应用。
4总结与展望
热化学储热技术在能源高效利用、保障能源系统安全稳定运行方面具有广阔的发展前景,在能源绿色低碳转型过程中发挥着重要作用。近年来,热化学储热材料发展迅速,但由于材料自身固有特性难以定向调控及改性工艺较为复杂等问题,致使材料性能尚未达到工业化应用的水平。因此,优质热化学储热材料的开发和应用仍面临诸多问题。
1)热化学储热材料种类较多,理化性质差异大,材料自身特性对储热应用场景具有决定性作用。因此,需要进一步发掘、优化完善储热材料体系,根据储热材料自身特性和应用场景需求,构建差异化热化学储热应用匹配方案,最大限度提高能量利用效率。
2)固体热化学储热材料普遍存在烧结、团聚、热导率低等问题。因此,优化传热传质特性,改善孔道结构和比表面积,提高颗粒强度,是提高固体储热材料储热密度和循环稳定性的关键。
3)对于氨、甲烷等气相热化学储热材料,反应过程中催化剂结焦和失活是影响其储热性能的关键因素。因此,开发低成本抗积碳催化剂,明确活性组分、载体种类和合成工艺对催化剂理化性能的影响,形成差异化的催化剂定向合成策略,耦合反应条件定向调控,实现气相储热材料的高效可逆转化,是未来推动气相热化学储热材料工业化的研究重点。
4)中高温热化学储热反应器设计及系统集成仍处于早期发展阶段,反应器存在导热性差、系统集成度低等问题。因此,亟待开发新型反应器,探究反应器内部物理和化学转化过程,阐明热质传递与化学反应之间的内在联系,优化反应器内构件设计,同时强化系统集成,通过多单元过程优化组合和耦合集成,提高系统能源转化和利用效率,并通过示范工程验证理论研究的可行性。
本文转自《热力发电》,作者:陈秋宇,李文涛,李竺豫,张怡,李胜,高丽娟,李凯。